DR.T 칼럼
약을 제조하고 유통하는 제약산업은 우리 생명과 직결되는 산업입니다.
원자재부터 제조과정, 포장에 이르는 모든 공정을 완벽하고 철저하게 관리해야 합니다.
이는 곧 제약산업의 품질 관리로 이어집니다.
제약산업, 철저하고 완벽한 품질 관리가 관건
세계 각국에서는 이러한 의약품의 안정성과 유효성을 지키기 위해
GMP(의약품 제조 및 품질관리기준)를 설정하고 이를 철저히 지키고 있습니다.
우리나라도 1990년대부터 GMP를 설정해 대부분의 제약회사는 이러한 기준을 따라
구조설비를 비롯해 원료의 구입에서부터 보관·제조·포장·출하에 이르기까지의
전 공정에 걸친 제조 및 품질관리를 시행하고 있습니다.
또한 인간의 평균 수명이 늘어남에 따라
국내 제약회사들은 당뇨, 암, 관절염 등
중증 만성 질환을 치료하는 바이오 신약 개발, 백신 생산에 적극적으로 나서고 있습니다.
바이오 기술과 접목한 제약산업은 연구에 집중하며 더욱 까다롭고
완벽한 공정 관리에 주의를 기울이고 있습니다.
특히 이 과정에서 온도와 습도 등 여러가지 환경 지표를 관리해야 합니다.
바로 이러한 환경 지표가 곧 의약품 및 바이오 관련 제품의
품질과 직결되기 때문입니다.

[ 제약 산업을 위한 중앙 모니터링 시스템 testo Saveris Pharma ]
그렇다면 이처럼 제약산업의 품질관리를 완벽하게 하기 위해서는 어떻게 해야 할까요?
제약산업의 전반적인 환경을 모니터링할 수 있는 솔루션이 필요합니다.
의약품, 혈액 제제 또는 백신을 연구하는 과정부터 생산하고, 보관, 유통되는
모든 과정을 지속적으로 관찰하고 기록해야 하기 때문이죠.
테스토의 제약산업을 위한 중앙 모니터링 시스템 testo Saveris Pharma 솔루션은
의약품의 품질에 중요한 영향을 미치는 대기 환경인
온도와 습도를 실시간으로 모니터링함으로써 품질 관리에 도움을 주는
깐깐하고도 확실한 시스템입니다.
연구 개발 단계부터 생산 및 보관, 유통까지
제약산업의 모든 과정을 책임지는 중앙 모니터링 시스템
제약 및 바이오 산업의 연구와 개발이 이뤄지는 연구실에서
환경 평가는 연구 활동을 뒷받침에 주는 중요한 요인입니다.
생산과정도 마찬가지입니다.
생산 과정의 온도와 습도가 어떻게 관리되느냐에 따라 결과물에 적지 않은 영향을 미칩니다.
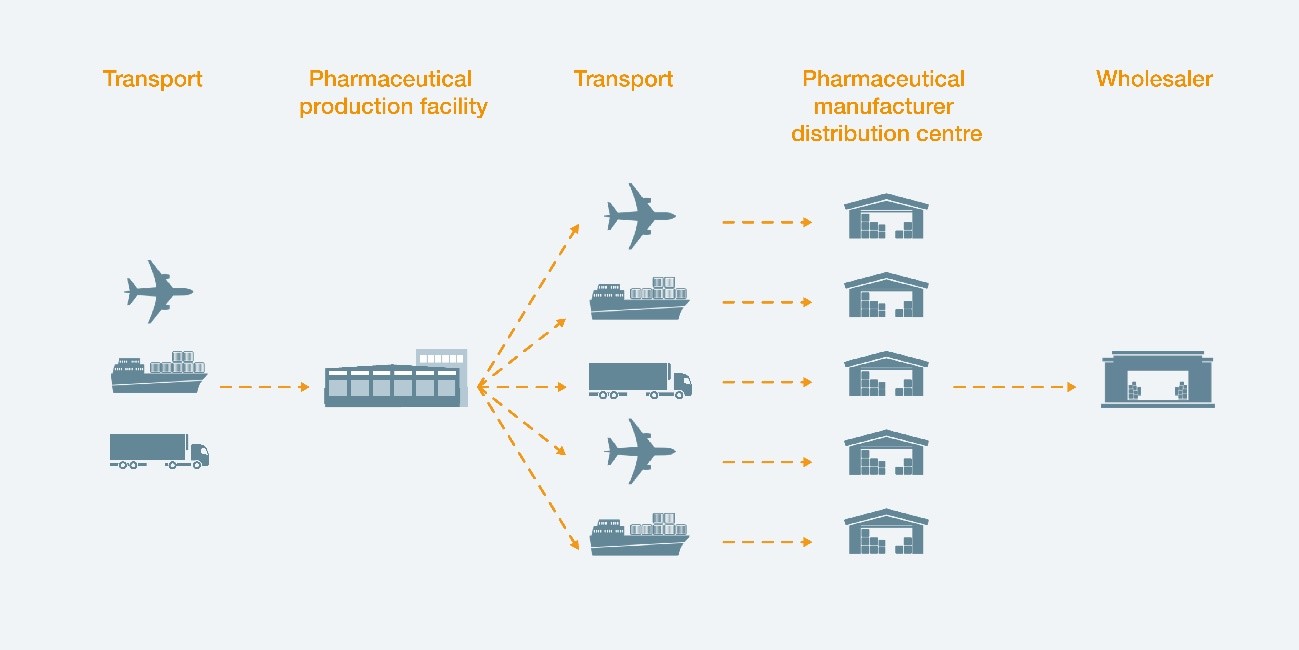
적절한 환경에서 생산된 제품을 이동하고 보관하는 것 또한 중요합니다.
운송이나 보관하는 과정에서 의약품이 변질될 우려가 있기 때문입니다.
예를 들어 사람의 체내 성분과 비슷한 백신, 인슐린, 혈액 등은 이동과정 중
최소 48시간, 최대 168시간 동안 온도, 습도, 충격 진동 등
모든 외부 위험 요인을 차단해야 합니다.

[ 무선 온습도 모니터링 시스템 testo Saveris Pharma 솔루션 ]
이러한 모든 과정에서 testo Saveris Pharma 솔루션은 완벽한 해결책이 될 수 있습니다.
제약산업의 품질 관리를 위한 중앙 모니터링 시스템 testo Saveris Pharma 솔루션은
1) 믿을 수 있는 측정 기술
2) 전문적인 CFR 소프트웨어
3) 종합적인 측정 서비스로 구성되어 있습니다.
즉 쉽게 말해 무선 측정 프로브나 유선 측정 프로브를
측정이 필요한 현장에 설치해두고,
베이스와 연결해 둔 PC를 통해 실시간으로 온도와 습도 등 환경 지표를
실시간으로 모니터링할 수 있습니다.
제약산업에 최적화된
컴퓨터 시스템 밸리데이션에 적합한 CFR 소프트웨어 지원

[ 미국 식품의약국 FDA(Food and Drug Administration) ]
특히 테스토의 제약 분야 솔루션인 testo Saveris Pharma는
컴퓨터 시스템 밸리데이션에 적합한 미국 FDA의 승인을 받은
21 CFR Part 11 소프트웨어를 지원하기 때문에 제약 분야에서 더욱 믿고 사용할 수 있습니다.
최근 의약품 및 바이오 산업의 규제가 까다로워지면서,
밸리데이션 문서화가 아주 중요한 화두로 떠오르고 있습니다.

[ testo Saveris CFR 소프트웨어 ]
testo Saveris CFR 소프트웨어는 FDA의 승인뿐 아니라,
독일의 대표적인 연구기관인 브라운호퍼 IESE (Institute for Experimental Software Engineering)의
인증을 받아 믿고 사용할 수 있습니다.
IESE는 testo Saveris CFR 소프트웨어가 전자 기록 및 전자 서명 측면에서
21 CFR Part 11의 기준을 충족한다는 것을 승인했습니다.
앞으로 바이오 기술이 발전함에 따라 제약산업은 전 세계 인류의 건강에
더욱 큰 영향을 미칠 전망입니다.
이때 테스토의 제약 분야 솔루션인 testo Saveris Pharma가 있다면,
제약산업의 전 과정에 걸쳐 꼭 필요한 품질 요건을 더욱 철저하고 완벽하게 지킬 수 있겠죠.
믿을 수 있는 제약 산업 뒤에는 믿을 수 있는 테스토의 솔루션이 함께하고 있습니다.
테스토 깜짝 상식

GMP(의약품 제조 및 품질관리기준)란?
의약품을 제조하는 공정에서 필수적으로 지켜야 할 관리 기준인 GMP(Good Manufacturing Practices)는
식품·의약품의 안정성과 유효성을 품질 면에서 보증하는 기본 조건입니다.
원료의 입고에서 출고까지 품질 관리 전반에 지켜야 할 규범이죠.
제약산업이 현대화, 자동화되며 제조시설과 엄격한 공정 관리로 착오를 줄이고 위생을 철저히 지킴으로써
안정성이 높은 고품질의 식품 및 의약품을 제조하는 데 목적이 있습니다.
Be Sure, Testo!

